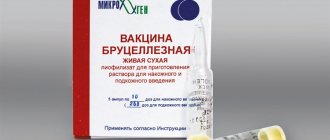
Данное сообщение (материал) создано и (или) распространено иностранным средством массовой информации, выполняющим функции иностранного агента, и (или) российским юридическим лицом, выполняющим функции иностранного агента.
Подпишите петицию с требованием отменить закон об иноагентах!
Весь мир с нетерпением ждет конца «нерабочих дней», периода «социального дистанцирования» или «локдауна» — в зависимости от того как в конкретной стране называют противовирусные меры. Однако Марк Липсич, профессор кафедры эпидемиологии Гарвардского университета, предупреждает — распространение болезни не остановится до тех пор, пока в популяции не будет достаточно уязвимых перед коронавирусом людей. Проще говоря, эпидемия не прекратится, пока большая часть из нас не переболеет — или пока не появится вакцина от коронавируса. Но почему же вакцины до сих пор нет? Давайте разбираться.
Все материалы «Медузы» о коронавирусе открыты для распространения по лицензии Creative Commons CC BY. Вы можете их перепечатать! На фотографии лицензия не распространяется.
На 30 апреля 2021 года сотрудникам Всемирной организации здравоохранения (ВОЗ) известно о 102 кандидатах в антикоронавирусные вакцины — причем восемь вакцин уже проходят клинические испытания на здоровых людях. Однако реальное число вакцин-кандидатов может быть больше: в список ВОЗ попали далеко не все компании, которые пытаются создать «волшебную пилюлю» против COVID-19.
Принцип действия уже существующих и еще только разрабатываемых вакцин основывается на нескольких способах вызвать в организме иммунный ответ, причем у каждого способа есть свои преимущества и недостатки. Предсказать, какой тип вакцин сработает лучше, до начала клинических испытаний на людях невозможно — так что фармацевтическим компаниям приходится действовать практически вслепую, пробуя разные способы. Но, может быть, это и к лучшему: если вакцины одного типа окажутся неэффективными или небезопасными, всегда есть шанс, что вакцины другого типа сработают лучше.
Глава 1
Вирусные вакцины
Вакцины на основе ослабленного вируса
Что это? Вакцина, в состав которой входит очень сильно ослабленный (иначе говоря, аттенуированный) в лаборатории вирус SARS-CoV-2. Вакцины такого типа известны с 1950-х годов: принцип лежит в основе прививок против кори, эпидемического паротита, краснухи (MMR) и ветряной оспы.
Каков механизм действия? Для создания вакцины сотрудники лаборатории используют вирус, которым последовательно заражают лабораторных животных. Дело в том, что вирусы приспосабливаются к тому хозяину, в чьем организме оказались. Если насильно «переселить» человеческий вирус в клеточную культуру животных, вирус начнет мутировать. Таким образом, после каждого цикла заражения вирус будет все лучше приспосабливаться к новому хозяину — и одновременно становиться все менее опасным для человека. При этом мутировавший «под животное» вирус остается все еще достаточно похожим на исходный «человеческий», чтобы вызвать у привитого человека полноценный иммунный ответ. Если привитый человек заразится исходным «диким» вирусом, его иммунная система уже будет готова к встрече и быстро справится с болезнью.
Что хорошего в этой вакцине? Иммунитет от такой прививки держится дольше всего. В случае COVID-19 это особенно важно, потому что к коронавирусным инфекциям не всегда формируется стойкий иммунитет.
В чем проблема с вакциной? Мы очень мало знаем о том, как мутируют вирусы, так что процесс создания «живой» вакцины во многом непредсказуем. Всегда есть шанс, что ослабленный вирус «вернет себе силу» и снова «научится» вызывать болезнь. Чтобы этого не произошло, приходится очень тщательно исследовать вирусы и организовывать скрупулезные клинические испытания полученной вакцины, которые займут несколько лет. Если удастся создать «живую» вакцину, у нее будет много преимуществ — но такой препарат появится еще не скоро.
Кто занимается вакциной и на каком она этапе? О начале разработки вакцины на основе ослабленного вируса американская компания Codagenix (разработка ведется совместно с Индийским институтом сывороток) объявила 13 февраля 2021 года. По данным ВОЗ, на 30 апреля 2021 года вакцина находится на фазе доклинических испытаний — то есть ее либо еще не создали, либо испытывают на лабораторных животных.
Как испытывают лекарства?
- Мне предложили участвовать в клинических исследованиях. Стоит ли на это соглашаться?
Инактивированные вакцины
Что это? Вакцина, в состав которой входят инактивированные — то есть не способные заражать клетки — вирусы. Это тоже старый и проверенный тип вакцин: принцип лежит в основе прививок от полиомиелита и коклюша.
Каков механизм действия? Чтобы создать вакцину, вирусы инактивируют — нагревают, обрабатывают ионизирующим излучением или дезинфектантами. Хотя белки «убитых» вирусов изменяют форму (то есть денатурируют), их химический состав остается прежним — а сами вирусные частицы отчасти сохраняют первоначальную форму. «Мертвые» вирусы тоже могут вызывать иммунный ответ.
Правда, у таких вакцин есть два недостатка. Во-первых, такие вакцины обычно вызывают слишком слабый иммунный ответ, так что приходится применять вещества — «усилители иммунной реакции» — адъюванты. Задача адъювантов — помочь иммунным клеткам (В-лимфоцитам) выработать больше защитных белков-антител.
В качестве универсального адъюванта в большинстве вакцин используют соли алюминия — однако вакцины с алюминием не помогают предотвращать вирусную инфекцию. Методом проб и ошибок ученые убедились, что противовирусные вакцины способны усиливать адьюванты-виросомы. Это «чучела вирусов» в виде липидных наночастиц — микроскопических капелек жиров-фосфолипидов, на поверхность которых «прицеплен» вирусный белок-антиген. Иммунные клетки принимают «чучела» за настоящие вирусы и реагируют на них более энергично, чем просто на вирусные белки-антигены.
Во-вторых, «учебный материал» для иммунной системы в конце концов заканчивается, так что полученный иммунитет не такой стойкий, как в случае вакцин на основе ослабленного вируса, способного некоторое время размножаться в организме. Чтобы поддержать иммунитет, приходится прибегать к повторной вакцинации.
Что хорошего в этой вакцине? Инактивированные вакцины безопаснее «живых» — ведь в них нет ослабленного вируса, который может мутировать.
В чем проблема с вакциной? Скорее всего, инактивированная вакцина к SARS-CoV-2 будет вызывать слабый иммунный ответ. Чтобы она работала хорошо, для нее придется подбирать эффективный адъювант — то есть искать оптимальные параметры фосфолипидной капли-виросомы. Это потребует дополнительного времени и усилий.
Кто занимается вакциной и на каком она этапе? По данным ВОЗ, на 30 апреля 2021 года наибольших успехов в создании инактивированной вакцины достигли два китайских разработчика. Компания Sinopharm готовит сразу две вакцины. Препарат, создаваемый в сотрудничестве с Уханьским институтом биопрепаратов (Wuhan Institute of Biological Products), находится на первой фазе клинических испытаний — переносимость вакцины проверяют на здоровых людях. Препарат, создаваемый совместно с Пекинским институтом биологических продуктов (Beijing Institute of Biological Products), находится в самом начале разработки — на этапе утверждения нормативных документов.
Больше всего информации об инактивированной вакцине от компании Sinovac, который тоже находится на первой фазе клинических испытаний. Эта компания сотрудничает с американской компанией Dynavax, которая передала Sinovac эффективный адъювант, хорошо показавший себя в вакцине против гепатита В — так что неудивительно, что китайский разработчик вырвался вперед, ведь это экономит ему массу времени.
19 апреля компания Sinovac опубликовала препринт — предварительный вариант статьи, в которой показала, что их вакцина работает: стимулирует образование антител против 10 штаммов SARS-CoV-2 у мышей, крыс и макак-резусов. Хотя радоваться все-таки рановато — мы еще не знаем, как вакцина покажет себя на людях.
Глава 2
О новых вакцинах от Covid-19
Каждая вакцина, основанная на платформе аденовирусных векторов имеет свои индивидуальные особенности, и прямое сравнение между ними является некорректным.
В частности, вакцина компании AstraZeneca использует вектор аденовируса шимпанзе для доставки антигена, состоящего из белка S, объединенного с лидерной последовательностью тканевого активатора плазминогена, — сообщают разработчики.
Вакцина от компании Johnson&Johnson использует вектор аденовируса человека 26-го серотипа и полноразмерный белок S, стабилизированный при помощи введения мутаций. Кроме того, её производство осуществляется в клеточной линии PER.C6 (это эмбриональные клетки сетчатки человека), которая не представлена широко среди зарегистрированных продуктов.
«Спутник V» – двухкомпонентная вакцина, в которой использованы серотипы аденовируса 5 и 26. В ней не используется фрагмент тканевого активатора плазминогена, а антигенная вставка представляет собой немодифицированный полноразмерный S-белок. Для производства вакцины «Спутник V» используется клеточная линия HEK293, которая уже давно применяется для производства биотехнологических продуктов.
Таким образом, все перечисленные выше вакцины на основе аденовирусных векторов имеют существенные отличия по структуре и технологии производства. В связи с этим, нет никаких оснований экстраполировать данные по безопасности, полученные в ходе использования одной вакцины – на данные по безопасности остальных вакцин.
Высочайшее качество и безопасность вакцины «Cпутник V» в том числе обеспечивается тем, что при производстве «Спутник V» в отличие от других вакцин используется технология 4-стадийной очистки, включающей две стадии хроматографической очистки и две стадии тангенциальной фильтрации. Такая технология позволяет получать высокоочищенный препарат, который проходит обязательный контроль на содержание остаточной ДНК в препарате, — уточняют в Центре Гамалеи.
Более того, в составе аденовирусных векторов содержится в десятки раз меньшее количество нуклеиновой кислоты по сравнению с вакциной Pfizer и Moderna (1-2 мкг в Спутнике V против 50 и 100 мкг в вакцинах Moderna и Pfizer, соответственно).
В исследовании, опубликованном в The New England Journal of Medicine 9 апреля 2021 года, обсуждается, что возможным триггером тромбозов у других препаратов может являться недостаточная очистка препаратов, вследствие чего в них может содержаться большое количество остаточной ДНК. При недостаточной очистке или использовании очень высоких доз целевой РНК/ДНК у других препаратов может происходить нежелательное взаимодействие антител пациента, активирующих тромбоциты, с элементами самой вакцины и/или остаточной ДНК/РНК, которые могут образовывать комплекс с фактором PF4.
Подробнее о вакцинах рассуждает Михаил Москвин Костин:
Цельновирионные инактивированные вакцины
Начнем с «классики», берущей свое начала во времена Дженнера и Пастера – цельновирионных (содержащие целые частицы вируса) инактивированных или живых вакцин, которые прекрасно себя зарекомендовали на протяжении столетий в борьбе с черной оспой, бешенством или корью. Все с такими вакцинами просто и понятно – убитый (инактивированный) или живой ослабленный (аттенуированный) вирус вводится пациенту, после чего он заболевает в легкой форме (живая вакцина) или выдает реакцию на вирусные частицы (инактивированный вирус). После этого у человека обычно формируется в той или иной степени стойкий гуморальный (антитела) и клеточный (Т-лимфоциты и другие клетки) специфический иммунитет к данному типу вируса. Достоинства очевидны – все происходит «естественным образом». Это имеет место при самом заболевании, но протекающем в легкой или абортивной (прерванной) формах. Иммунитет же получается комплексный и прочный настолько, насколько он вообще может быть прочен по отношении к данному инфекционному агенту. Недостатки являются прямым продолжением достоинств метода – у людей бывают реакции, вполне сопоставимые с самой болезнью, могут возникать осложнения, характерные для самой болезни. Вакцины «жесткие», но в периоды эпидемий чаще всего самые применимые и необходимые.
Сегодня цельновирионные инактивированные вакцины в трех лабораториях уже подготовил к широкому внедрению Китай (Sinovac; Beijing Institute of Biological Products/Sinofarm; Wuhan Institute of Bioliogical Products/Sinofarm). В нашей стране такую вакцину подготовил к широкому применению Федеральный научный центр исследований и разработки иммунобиологических препаратов имени М.П.Чумакова РАН. (ФГБНУ ФНЦИРИП им. М.П. Чумакова РАН, далее и везде «Центр им. Чумакова»), традиционно специализирующийся на живых и инактивированных «классических» вакцинах».
Рекомбинантные вакцины
Относительно инновационными вакцинами (широкое использование которых насчитывает «всего лишь» пару десятков лет) являются векторные вакцины, в том числе, сделанные на «аденовирусной платформе». На них надо остановиться особо, так как к ним относится уже готовая к широкому применению в России вакцина «Спутник V». Разработанная и внедренная Национальным исследовательским центром эпидемиологии и микробиологии имени почётного академика Н. Ф. Гамалеи Министерства здравоохранения России (ФГБУ НИЦЭМ им. Н. Ф. Гамалеи Минздрава России, далее и везде «НИЦ им. Гамалеи»).
Для создания таких вакцин используется, в частности, измененный ДНК-содержащий вирус ОРВИ человека – аденовирус, относящийся к безопасным серотипам (иммунологически выявляемым типам) 5 и 26 (Ad5, Ad26). Данные вирусы широко распространены в различных странах (особенно, 5 серотип) и вызывают обычно быстропроходящие сезонные заболевания, чаще всего, в виде насморка, катара верхних дыхательных путей, небольшого шейного лимфаденита или кишечного расстройства (так называемый, «летний грипп»).
Этот вирус пригоден для использования в виде «вектора» – носителя, позволяющего доставить в клетки необходимую для иммунизации важную последовательность ДНК, кодирующего белки совсем другого вируса, в данном случае коронавируса 2 (SARS-CoV-2), вызывающего COVID-19. Получается комбинация, которую мы иногда в лаборатории называли «путник в лодочке». Где «лодочкой» является измененный аденовирус, а «путником» – фрагмент ДНК, кодирующий S-белок шипа (spike) вирусной частицы. Которые и образуют «корону» вокруг оболочки (нуклеокапсида) коронавируса. Именно к этой «короне» мы и должны получить после иммунизации нейтрализующий коронавирус антитела. Вот такой «гибрид», искусственно сделанный из двух вирусов – аденовируса и коронавируса.
При этом, безопасности ради, из аденовируса убирается важный фрагмент ДНК его генома, ответственный за инициацию за его размножения внутри клеток (вирусы – внутриклеточные паразиты, сами к размножению вне клеток неспособны). Однако такой аденовирус-вектор сохраняет способность инициировать в зараженных им клетках производство по его матрице не только «лодочки» своих аденовирусных белков, но и материала «путника», то есть S-белка шипа коронавируса. Каждая зараженная таким «гибридным» вирусом-вектором клетка, например, слизистой оболочки носа не становится «поточным цехом» по производству аденовируса, но выполняет роль небольшой «фабрики по производству» S-белка коронавируса, которая необходима для выработки долгосрочного иммунитета к нему.
Таким образом, аденовирус-вектор попадет в организм, внедряется в клетки, но не вызывает их гибель, а обеспечивает производство важного для иммунизации антигена на протяжении многих дней и даже недель. Организм распознает S-белок вируса и постепенно вырабатывает антитела к нему в течение примерно 14 – 28 дней после иммунизации. Параллельно происходит и тонкая настройка клеточного иммунитета. Такая иммунизация проходит обычно спокойнее и «нежнее», чем при использовании классических вакцин, а иммунитет получается обычно прочный и качественный.
Правда, иногда бывают сбои, ведь «где тонко, там и рвется». Так, если человек недавно переболел аденовирусом данного Ad5 или Ad26 типа, и у него есть активный иммунитет именно против него. В этом случае «лодочка» будет обнаружена антителами и «потоплена» еще до того, как успеет доставить «путника» по назначению. Также может быть ситуация, когда сразу после прививки человек заразится любым другим аденовирусом, «летним гриппом», который кочует в популяции. «Дикий» аденовирус «поделится» продукцией отсутствующего в нашей «лодочке» гена, и наш, исходно неспособный к размножению вектор, станет на время снова реплицирующим вирусом, тоже начнет воспроизводиться в зараженных клетках. В этом случае иммунный ответ может быть изменен, искажен или неожиданно усилен (интерференция вирусов). И та, и другая ситуация возможны, но, как установила многолетняя практика, опасности осложнений это обычно не влечет. Любая вакцинация таит в себе риски, но в случае рекомбинантных вакцин на базе аденовирусов она сводится к минимуму. Да, есть реакции от прививок такими вакцинами: температура, слабость и прочее на уровне, обычно по тяжести близкой к вакцинам для взрослых от сезонного гриппа.
Перейдем к текущей ситуации. В мире сейчас предлагаются широкому использованию четыре рекомбинантных вакцин:
• Американская (Janssen Pharmaceutical Companies) на основе платформы Ad26.
• Китайская (CanSino Biological Inc./Beijing Institute of Biotechnology) на платформе Ad5.
• Российская «Спутник V» (Центра им. Гамалеи) сразу на двух платформах Ad5 и Ad26
• Британско-шведская вакцина (University of Oxford/Astra Zeneca) в основу которой положен не человеческий материал, а выбраны в качестве «лодочки» для доставки «путника» в клетки аденовирусы приматов (шимпанзе).
Зачем англичане взяли в качестве платформы аденовирусы приматов понятно. Иммунитет человека никогда не встречался с «ковидными» вирусами, он их не может узнать, «лодочка» не будет подтоплена, и с вероятностью близкой к 100% доставит «путника» (ген, кодирующую S-белок коронавируса) по месту назначения – в клетки эпителия слизистой оболочки, на которых имеется маркер – белок SARS, нужный для внедрения в них аденовирусного вектора.
В случае китайской вакцины проблема такая, что «лодочка» – вектор Ad5, будет «потоплена», то есть вакцина инактивирована иммунитетом, весьма велика, так как данный серотип очень распространен. Для американской вакцины на основе Ad26 такая вероятность много меньше, но существенна. Российские же ученые пошли по особому пути: поскольку вакцинация векторными вакцинами проводится дважды (первичная и добавочная «бустерная»), то выбраны обе платформы – и Ad5 и Ad26, что повышает вероятность благополучной иммунизации, но все же не делает ее 100%.
Вроде шведско-британская вакцина в плане доставки в клетки надежнее всех трех других – российской, китайской и американской, но ее «происхождение от обезьяны» заставляет немного задуматься: в организм человека попадет вирусный материал другого вида, который в случае интерференции вирусов или мутации самого вируса обезьяны в человеческом организме может дать неожиданные результаты. Есть в этом тревожные моменты, хотя практика британских ученых показала, что вроде бы такая платформа опасности для пациентов не несет. Но все когда-то случается впервые.
Однако, если бы мне предложили пройти при отсутствии выбора иммунизацию против коронавируса одной из описанных выше четырех рекомбинантных вакцин, я бы согласился на любую из них. Имея же такой выбор, остановился бы на «Спутнике V» – и гарантии доставки выше, чем у китайцев и американцев, и материал человеческий, а не взятых у наших дальних родственников из африканского леса. Так что, касательно рекомбинантных вакцин – они все родственны между собой, уровень безопасности у них примерно одинаковый, а то, что периодически кто-то берется что-то иное утверждать о вакцине «Спутник V» – это всего лишь следствие конкурентной борьбы или заблуждений, не более того. Все эти четыре вакцины вполне надежны.
Теперь о следующей вакцине, в этом разделе, она одна – «ЭпиВакКорона». Разработанная, испытанная и уже внедряемая в гражданский оборот Федеральным бюджетным учреждение науки «Государственный научный центр вирусологии и биотехнологии „Вектор“» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ГНЦ ВБ «Вектор», далее и везде «Центр Вектор»). Эта вакцина содержит только фрагменты самого S-белка коронавируса, в ней нет никакого генетического материала из каких-либо вирусов или клеток.
Три фрагмента S-белка вируса SARS-CoV-2 «пришиты» к некой белковой основе и иммобилизованы на частицах гидроокиси алюминия, (выполняющих роль вспомогательного раздражителя для выработки иммунитета — адъюванта). Вакцина «нежная», спокойная, но, вероятно, не такая сильная, как классические или рекомбинантные, описанные выше, особенно в части создания клеточного иммунитета. Подобная «мягкость» и некоторая односторонность вакцины в некоторых случаях могла бы вызвать и некоторую настороженность. Дело в том, что при ряде вирусных заболеваний, вызываемых некоторыми вирусами (в том числе, родственным коронавирусом (SARS-CoV) острого легочного дистресс-синдрома – «атипичной пневмонии» 2002-2003 годов в Юго-Восточной Азии). У лиц, которые не смогли сформировать при первом контакте с вирусом или после первой вакцинации от такого вируса полноценного иммунитета, иногда наблюдается синдром усиления болезни при повторном заражении или же заражении после неэффективной прививки (antibody-dependent enhancement, ADE). Слишком (мягкая) прививка, защищающая лишь частично, в случае коронавируса теоретически может таить в себе такую же опасность.
Для Covid-19 такое утяжеление течения болезни при повторном заражении или после неэффективной прививки пока достоверно не показано и даже опровергается, тем не менее, с учетом родства вирусов атипичной пневмонии SARS-CoV и нашего вируса SARS-CoV-2, расслабляться не следует.
Надо будет тщательно отслеживать ситуацию с течением Covid-19 в том случае, если вдруг у кого-то заболевание возникло вскоре после прививки. Нельзя терять бдительность в этом вопросе. Если меня сегодня спросят, что бы я предпочел для себя, я выбрал бы, наверное, «Спyтник V» НИЦ им. Гамалеи, хотя также спокойно сделал бы прививку и «ЭпиВакКорона» , так как не считаю риск ADE значительным. «ЭпиВакКорона» сегодня рекомендуется специалистами лицам пожилым и больным людям, с аллергическими заболеваниями, как самый «мягкий» и щадящий вариант вакцинации. Также, следует отметить особую роль, которую «ЭпиВакКорона» может сыграть в будущем при ревакцинациях, где ее гипотетические минусы обращаются в очевидные плюсы, на чем остановлюсь ниже отдельно.
Вакцины на основе мРНК
И вот, наконец, трубно и победно звучащие две американские вакцины (BioNTech\Fosun Pharma/Pfiser; Moderna\NIAID) на основе мессенджер-РНК (информационных РНК, мРНК), кодирующих все тот же самый S-белок шипа коронавируса, и также, как в случае с рекомбинантными вакцинами, доставляемых в клетки организма в «лодочках» из липидных наночастиц.
Вакцины на основе мРНК, синтезируемых в промышленных масштабах, представляется делом весьма перспективным, хотя и неизведанным. У них есть большие преимущества перед многими другими в части стимуляции иммунитета вообще без контакта организма человека с вирусами. Такая вакцина также является «путником в лодочке» – в качестве «лодочки» обычно берется наночастица, микровезикула, «пузырёк», в котором едет «путником» мРНК, кодирующая синтез только одного единственного белка. Клетки, в которые мРНК попадает, при этом не разрушаются, продукция белка длится несколько дней, формируется хороший клеточный и гуморальный иммунитет. Все замечательно. Даже то, что такая вакцина стоит в 5 – 10 раз дороже, чем рекомбинантная или цельновирионная, и требует особых условий транспортировки, хранения и применения внутри «непрерывной холодовой цепи» (-70 С), не снижает ее значения – здоровье дороже.
Такие вакцины на основе мРНК, также, как и рекомбинантные векторные, о которых уже говорилось выше, уже разрабатываются на протяжении почти 30 лет, с начала 1990-х годов. Они модифицируются, усовершенствуются и испытываются на хлопковых хомячках, яванских макаках, хорьках, морских свинках, показывают хорошие результаты при лечении везикулярного стоматита у белых мышей.
Настораживает другое. Такие вакцины пока в массовом порядке не применялись не только для профилактики инфекционных заболеваний людей, но и для иммунизации сельскохозяйственных животных (не считая отдельных опытов по иммунизации собак против бешенства и свиней для получения антител против вируса гриппа). Но обе американские компании с большой быстротой за 9 месяцев создали и довели до регистрации системы производства мРНК- вакцин против S-белка SARS-CoV-2. По данным американских источников обе вакцины показала высокую эффективность во всех группах испытуемых в целом ряде стран, независимо от того, какого возраста, пола или расы были привитые ею люди. При этом для людей старше 65 лет эффективность одной из этих вакцин составила 94%. Пожилые легче переносили прививку, реже жаловались на побочные эффекты. Имеется в виду, конечно же, ближайшие по времени побочные эффекты, но не отдаленные, о существовании или же об отсутствии которых для вакцин на основе мРНК нет данных по описанным выше причинам. И это тоже несколько тревожит.
Вернуться
Векторные вакцины
Что это? Вакцины на основе совершенно иных вирусов (например, аденовирусов), в которые встроен небольшой ген — участок генома SARS-CoV-2. В результате в составе оболочек безобидных вирусов (их называют «вектором», то есть транспортом для доставки в клетки) появляются белки-антигены SARS-CoV-2.
Каков механизм действия? Попав в организм вместе с вакциной, генетически модифицированные вспомогательные вирусы провоцируют иммунный ответ на белки SARS-CoV-2 — то есть работают примерно как «живые» вирусные вакцины.
Теоретически можно попытаться создать векторные вакцины двух типов — на основе способных и не способных размножаться в организме вирусных частиц. Скорее всего, вакцины на основе вирусных частиц, способных к размножению внутри клеток организма-хозяина, будут дольше защищать от коронавируса. Однако до стадии клинических испытаний на людях пока дошли только вакцины с вирусами, к размножению не способными.
Что хорошего в этой вакцине? Согласно замыслу разработчиков, векторные вакцины должны работать так же хорошо, как живые, — но при этом не смогут мутировать.
В чем проблема с вакциной? Векторные вакцины на основе ослабленного генно-модифицированных аденовирусов недостаточно изучены. Попытки разработать векторные вакцины для борьбы с раком, вирусами ВИЧ, гриппа и Эболы уже предпринимались, но пока ни одна не была одобрена для людей.
Кто занимается вакциной и на каком она этапе? По данным ВОЗ, на 30 апреля 2021 года векторными вирусными вакцинами занимаются два сильных игрока.
Китайская компания CanSino Bio совместно с Пекинским биотехнологическим институтом (Beijing Institute of Biotechnology) разрабатывает вакцину Ad5-nCoV — на основе модифицированного аденовируса 5-го типа. Вакцина находится во второй фазе клинических испытаний — то есть уже начались испытания вакцины на реальных пациентах. На данный момент CanSino Bio лидирует в «вакцинной гонке» — но это пока ни о чем не говорит, ведь результатов первой фазы испытаний мировое медицинское сообщество до сих пор не видело. Не исключено, что с вакциной есть целый ряд не заявленных проблем.
Второй сильный игрок — английский Оксфордский университет (University of Oxford), который разрабатывает векторную вакцину на основе модифицированного аденовируса шимпанзе ChAdOx1. Вакцина находится на 1–2-й фазе клинических испытаний — то есть ее тоже уже тестируют на реальных пациентах. О ChAdOx1 пока особенно ничего не известно. Но другой оксфордский продукт, основанный на том же принципе — вакцина против MERS-CoV, «двоюродного брата» вируса SARS-CoV-2, — вроде бы работает, и проблем с безопасностью у нее не было.
Глава 3
Производство и описание вакцины
Ранее был представлен процесс выделения и генетического описания вакцинного штамма AYDAR-1 [21]. Вирус удалось профильтровать на третьем пассаже и дополнительно очистить путем разбавления. Были созданы первичные, основные и рабочие посевные серии штамма (а именно пассажи под номерами 7, 8 и 9), которые были охарактеризованы в соответствии с национальными руководствами по производству вакцин.
Рисунок 1 | Процесс производства вакцины «КовиВак» и установление ее подлинности
A — Основная последовательность процесса производства вакцины; B — Трансмиссионная электронная микроскопия (ТЭМ) с негативным контрастированием концентрата инактивированной вакцины после хроматографической очистки; выделенная частица (внизу справа); C — Электрофорез (SDS-PAGE) вакцинного препарата (очищенный инактивированный вирусный препарат после хроматографии), окрашенный кумасси синим; D — Вестерн-блоттинг вирусного препарата перед инактивацией и вакцинный препарат (очищенный инактивированный вирусный препарат после хроматографии), окрашенный сывороткой человека-реконвалесцента после COVID-19; E — Вестерн-блоттинг препарата вируса перед инактивацией и приготовлением вакцины (очищенный препарат инактивированного вируса после хроматографии), окрашенный анти-S-белковой сывороткой кролика; F — культура клеток Vero, инфицированных SARS-CoV-2 и окрашенных сывороткой мыши, иммунизированной вакциной «КовиВак» (зеленое окрашивание на микрофотографии) и Hoechst 33342 (синее окрашивание на микрофотографии); G — клетки Vero, инфицированные SARS-CoV-2 и окрашенные сывороткой человека-реконвалесцента после COVID-19 (зеленое окрашивание) и Hoechst 33342 (синее окрашивание).
Благодаря трансмиссионной электронной микроскопии (ТЭМ) (рис. 1B) с негативным контрастированием концентратов были обнаружены плеоморфные сферические вирусные частицы диаметром около 120 нм, покрытые шиповидными структурами длиной 16–20 нм.
Методом ТЭМ (рис. 1B) были подтверждены гомогенность и чистота вакцинного препарата и выявлены вирионы с шипиковыми белками, соотносящиеся по форме и размеру с таковыми, выявляемыми в других исследованиях [26, 27].
В ходе электрофореза SDS-PAGE и вестерн-блоттинга (ВБ) концентратов вакцин перед инактивацией и после хроматографии, окрашенных сыворотками реконвалесцентов после COVID-19 (рис. 1 C и D), были выявлены два основных белка в концентратах: N и S, которые должны содержаться и в препарате вириона. С помощью окрашивания сывороткой анти-S-белка (рис. 1E) были обнаружены две формы S-белка в вирусных препаратах до и после инактивации: S1 и полноразмерный S-белок. Это свидетельствует о том, что в вакцинном препарате присутствует антиген-мишень для индукции синтеза НАт.
Специфичность реактивности антител подтверждается отсутствием свечения (флуоресценции) в неинфицированных клетках культуры Vero.
Вакцины на основе нуклеиновых кислот
ДНК-вакцины
Что это? Вакцина, которая содержит кольцевую молекулу ДНК (плазмиду), в которой записаны «инструкции» по созданию вирусного белка.
Каков механизм действия? Попав в клетки привитого человека, кольцевая ДНК станет частью их генома. В результате клетки организма-хозяина получат новую инструкцию, по которой начнут «штамповать» вирусные белки-антигены — и на них будет формироваться иммунный ответ.
Чтобы кусочек ДНК с информацией о вирусных белках наверняка проник в клетки, его можно встроить в геном безобидного вируса-носителя. Этот вирус работает как «внутриклеточный шприц» — забрасывает в клетку свой модифицированный геном, который потом встраивается в ядро (в отличие от векторных вакцин, здесь от безобидного вируса используется только оболочка).
Что хорошего в этой вакцине? Преимущества такие же, как у векторных вакцин: иммунитет такой же стойкий, как у «живых» вирусных вакцин, но без присущих им недостатков. Поскольку в качестве «вируса-носителя» для плазмиды берется совсем не SARS-CoV-2, нет опасности, что ослабленный вирус мутирует и снова будет вызывать болезнь.
В чем проблема с вакциной? ДНК-вакцины плохо изучены. Пока применяется всего одна вакцина такого типа — прививка от вируса Зика для лошадей. Ни одна ДНК-вакцина пока не получила разрешения для использования на людях.
Кто занимается вакциной и на каком она этапе? По данным ВОЗ, на 30 апреля 2021 года компания Inovio Pharmaceuticals (Пенсильвания, США) создает ДНК-вакцину INO-4800 — только на основе ДНК-плазмид, без модифицированных вирусов-носителей. INO-4800 — так называемая ДНК-вакцина с электропорацией. Чтобы «загнать» плазмиду в клетки мышц или кожи, на них нужно будет воздействовать электрическим полем, которое на время сделает клеточные мембраны более проницаемыми. Чтобы сделать такую прививку, простого шприца будет недостаточно — потребуется специальный прибор-электропоратор. Эта вакцина находится в первой фазе клинических испытаний — результаты испытаний ожидаются в июне.
РНК-вакцины
Что это? Вакцина, которая содержит вирусную молекулу, по структуре похожую на ДНК — матричную РНК (мРНК). Эта молекула — «шаблон», с которого напрямую считывается вирусный белок. В клеточный геном мРНК не встраивается.
Каков механизм действия? Заключенная в липидную наночастицу мРНК попадает в организм вместе с вакциной. Затем липидная частица сольется с мембраной клетки-мишени, а ее содержимое попадет в клетку и превратится в «шаблон» для синтеза вирусных белков-антигенов. В результате собственные клетки организма начнут синтезировать вирусные белки — притом что вирусная ДНК в клеточный геном встраиваться не будет.
Что хорошего в этой вакцине? Помимо преимуществ, общих с ДНК-вакцинами, липидные частицы с мРНК внутри похожи на вирус, так что сами по себе могут вызывать иммунный ответ. Есть шанс, что из-за «двойного действия» иммунитет от РНК-вакцин будет возникать раньше и держаться крепче. Кроме того, короткая мРНК — очень простая молекула, поэтому создать ее можно относительно быстро и недорого — с помощью специальных синтезаторов.
В чем проблема с вакциной? Это абсолютно новая вакцина — так что мы понятия не имеем, как она будет себя вести в человеческом организме. Более старых вакцин подобного типа в принципе не существует.
Кто занимается вакциной и на каком она этапе? По данным ВОЗ, на 30 апреля 2021 года в создании РНК-вакцин дальше всего продвинулись две компании. Американская компания BioNTech заключила контракт с фармацевтическим гигантом Pfizer. Однако помимо того, что компания получила разрешение на начало 1–2-й фазы клинических испытаний в Германии, о вакцине известно мало. Тем не менее представители сообщили, что их вакцина может быть готова уже к осени 2021 года.
Больше информации о вакцине от американской компании Moderna, которая сотрудничает с Научно-исследовательским центром вакцин (NIAID). Вакцина называется мРНК-1273. Недавно закончилась первая фаза испытаний, в которой участвовало три варианта вакцины с концентрацией мРНК 25, 100 и 250 микрограмм. Сейчас компания подала заявку на вторую фазу испытаний, в которой будет участвовать вакцина в дозировках 50 и 250 микрограмм — возможно, именно такие дозировки оказались наиболее эффективными.
Кроме того, в середине марта о начале разработки РНК-вакцины объявила российская биотехнологическая компания BIOCAD. Разрабатываться будет три варианта вакцины с разными дозировками мРНК. Первые испытания на животных планировалось начать в конце апреля.
Глава 4
Белковые вакцины
Что это? Вакцина на основе белков-антигенов, то есть «кусочков» вируса.
Каков механизм действия? Попадая в организм вместе с вакциной, смесь вирусных белков-антигенов провоцирует иммунный ответ.
Что хорошего в этой вакцине? Такая вакцина безопасна для организма — поэтому ее можно быстро протестировать и пустить в дело.
В чем проблема с вакциной? Очень сложно получить достаточно вирусных белков, чтобы хватило на вакцину. Кроме того, иммунитет к таким вакцинам, скорее всего, будет нестойким — примерно как в случае инактивированных вакцин.
Кто занимается вакциной и на каком она этапе? По данным ВОЗ, на 30 апреля 2021 года ни одна белковая вакцина еще не перешагнула порог доклинических испытаний. А если и перешагнет, то маловероятно, что такие вакцины станут массовыми. Хотя в теории возможность производства вирусных белков в большом количестве существует — например, у компании Sanofi есть технология, позволяющая «штамповать» белки вирусов гриппа в клетках гусениц. Но делать вакцины таким способом очень дорого и сложно.
Глава 5
Иммунитет и его стойкость
Краткосрочная иммуногенность вакцины «КовиВак» была оценена на трех животных моделях (двух генетических линиях мышей, сирийских хомячках и обыкновенных игрунках), иммунизированных разными дозами. Вакцина индуцировала синтез НАт у всех изученных видов. Более того, у мышей были обнаружены антитела к двум основным структурным белкам вируса (S и N). В течение первых 2–4 недель не наблюдалось значительных различий между титрами НАт, синтез которых был вызван различными дозами антигена. Различия проявились начиная с пятой недели после первой иммунизации.
Как было отмечено выше, синтез НАт является одним из основных маркеров защиты от SARS-CoV-2 [8]. Следовательно, длительность антительного ответа (НАт) коррелирует с длительностью защиты. После естественного заражения, особенно в случае легкого течения инфекции, ответ в виде НАт довольно слабый и непродолжительный [11].
Сведений об устойчивости иммунитета, вызванного вакциной, очень мало. Хотя в опубликованных доклинических исследованиях показана индукция титров IgG и НАт к SARS-CoV-2 IgG вследствие введения различных вакцин, лишь в немногих работах содержатся данные о продолжительности иммунного ответа. Например, для препарата PiCoVacc (инактивированная вакцина), опубликованы результаты доклинических испытаний, согласно которым титр антител после вакцинации мышей и крыс сохраняется в течение шести недель, а у макак-резусов — до трех недель [25]. В работе, опубликованной Wang с соавт., анализ иммуногенности у животных был ограничен четырьмя неделями [27].
В случае вакцины-кандидата BBV152 измерение иммуногенности при трехдозовом режиме введения проводилось до 25-го дня [29]. Авторы провели оценку долгосрочной иммуногенности у мышей и игрунок в течение одного года. За этот период значительного снижения титров НАт обнаружено не было. Более низкие дозы вводимого антигена приводили к формированию более низкого титра НАт в течение длительного периода наблюдения. Хотя очевидно, что окончательные сведения о длительности иммунитета, обеспечиваемого вакцинами против COVID-19, будут получены в ходе длительных клинических исследований, в данной ситуации животные модели могут служить в качестве удобных суррогатных индикаторов на ранних этапах процесса разработки вакцины. В недавней работе, посвященной клиническому исследованию вакцины на основе мРНК компании Moderna, сообщается о существовании повышенного титра специфических антител в течение как минимум трех месяцев [30]. Согласно экспериментальным данным авторов статьи, вакцина «КовиВак» обеспечивала формирование стабильного длительного иммунитета у мышей и игрунок после двухкомпонентного режима введения препарата.
Почему вакцины разрабатывают так долго
Создавать вакцины очень сложно и дорого. Создание вакцин требует не только высококвалифицированных кадров и больших финансовых вложений в исследования — проблема еще и в налаживании производства. Чтобы вывести вакцину на рынок, небольшие компании-разработчики должны будут договориться с крупными фармацевтическими компаниями, которые смогут выпускать компоненты для лекарства крупными партиями. При этом производство вполне эффективной вакцины может оказаться слишком сложным, чтобы стать массовым — мы уже видели это на примере белковых вакцин. Из-за производственных сложностей до потребителей не доходит 95% вакцин, успешно прошедших клинические испытания.
Клинические испытания вакцин занимают много времени. Успешная вакцина — препарат, который будет применяться у десятков тысяч, а возможно, и миллионов людей. Поэтому все кандидаты в вакцины должны проходить тщательную проверку не только на эффективность, но и на безопасность — ведь при таких огромных объемах даже редкие побочные эффекты становятся весьма вероятными.
Хороший пример — риск антителозависимого усиления инфекции (ADE), при котором возникает теоретический риск, что антитела из вакцины, предназначенные для борьбы с одним штаммом коронавируса, будут облегчать инфекцию другим штаммом коронавируса. Ученые не до конца понимают, какие именно свойства вакцин провоцируют ADE — поэтому приходится просто экспериментировать и смотреть, есть ли этот эффект или его нет. Проверка на ADE тоже занимает время.
И хотя разработчики вакцин (особенно новых — векторных и вакцин на основе РНК и ДНК) делают все, чтобы ускорить процесс разработки, этап проверки вакцин на людях — клинические испытания — пропускать ни в коем случае нельзя.
Клинические испытания (даже ускоренные) занимают минимум несколько месяцев. Требуется набрать несколько десятков (а лучше сотен) участников, случайным образом (это называется рандомизация) разбить их на опытную группу, которая получит вакцину, и контрольную группу, которая получит плацебо, и наблюдать за этими людьми как минимум 3–4 месяца, чтобы успели проявиться возможные побочные эффекты.
Глава 6
Профилактическая эффективность
В большинстве недавних исследований в качестве удобной и достоверно нелетальной животной модели профилактической эффективности вакцин против COVID-19 используется золотистый (сирийский) хомячок. У сирийских хомячков инфекция SARS-CoV-2 вызывает значительные патологические изменения в легких и, таким образом, поддерживает развитие стабильного постинфекционного гуморального иммунного ответа в экспериментах с пассивным переносом [35]. Более того, наблюдаемые иммуногистохимические изменения и характер потери массы тела у хомячков сходны с легкой формой инфекции SARS-CoV-2 у человека [36]. В ряде работ продемонстрирована пригодность сирийского хомячка в качестве модели для изучения профилактической эффективности НАт и вакцин против SARS-CoV-2 [37–46], хотя симптомы пневмонии у животного развиваются быстро и протекают тяжело.
Сирийский хомячок в качестве модельного объекта был использован для оценки профилактической эффективности нескольких инактивированных вакцин [47–48], в том числе одобренных для клинического применения [29]. К основным параметрам оценки относят вес животного и присутствие вируса и/или вирусной РНК в мазках из носа, легких и других органов в разные сроки после инфицирования.
В исследовании авторов животные из группы контроля теряли вес до пятого — седьмого дня с момента заражения, тогда как вакцинированные набирали вес с начиная с третьего дня после заражения, что соотносится с данными о BBV152 [29]. Однако потеря веса у контрольных животных в экспериментах авторов была более выраженной — 15 % против 2–10 % в исследовании BBV152. Скорость выведения вирусной РНК из верхних дыхательных путей также была сходной: начиная с седьмого дня после инфицирования в большинстве мазков из носа вирусная РНК не содержалась. Уровень вирусной РНК в легких контрольных животных был одинаковым в обоих исследованиях; по данным авторов, в органах всех контрольных животных содержалась вирусная РНК на четвертые, седьмые и 14-е сутки. Ткани легких вакцинированных животных в основном не содержали вируса: только у одного из пяти хомячков на четвертый и седьмой дни можно было выявить РНК вируса в легких; однако к 14-му дню ткань легких очищалась от вируса. Вирусная РНК была обнаружена в иных тканях (помимо легочной) у животных контрольной группы только на третий день после заражения. Аналогичные результаты были получены для вакцинного препарата BBV152 [29]. Таким образом, представленные результаты демонстрируют профилактическую эффективность вакцины «КовиВак» на модели сирийского хомячка.
Таким образом, для вакцины «КовиВак» не было обнаружено признаков острой/хронической, репродуктивной, эмбрио- и фетотоксичности или тератогенного влияния в антенатальном и постнатальном периодах развития, а также признаков гиперчувствительности у исследованных видов животных. Вакцина способствовала формированию стабильного и устойчивого гуморального иммунного ответа — как в виде специфических IgG к SARS-CoV-2, так и НАт у грызунов и обезьян. Значительного снижения титров НАт в течение одного года не наблюдалось. «КовиВак» продемонстрировала профилактический эффект по отношению к инфекции SARS-CoV-2 у сирийских хомячков. Эти данные стимулируют дальнейшее изучение вакцины «КовиВак» в клинических испытаниях.
Когда ждать появления вакцины
В «докоронавирусную эру» разработка одной вакцины в среднем занимала более 10 лет. Единственное исключение — вакцина против вируса Эбола: с разработкой этого лекарства компания Merck справилась за рекордные пять лет. Но в разгар пандемии COVID-19 такого количества времени нет ни у одной из стран мира, поэтому регулирующие государственные органы и фармацевтические компании ускоряют разработку и тестирование кандидатов в вакцины — например, правительство США надеется получить готовое лекарство к началу 2021 года.
Если подобное действительно получится, это будет невиданный шаг вперед для всего человечества. Однако это все-таки не слишком вероятно. Учитывая все вышеизложенное, вакцину от COVID-19 не имеет смысла ждать раньше чем через 12–18 месяцев.
Кстати, недавно появился специальный сайт, который агрегирует информацию от ВОЗ, американских Центров по контролю и профилактике заболеваний CDC и из других источников: COVID-19 Vaccine & Therapeutics Tracker. На сайте удобно следить за разработкой вакцин в реальном времени.