Российские вакцины
Сегодня в России для профилактики коронавирусной болезни и ее осложнений используются только отечественные препараты. Это вакцины следующих типов:
- Векторные. Генно-инженерные вакцины, где в качестве вектора выступает безопасный для человека вирус. В него вставляют ген одного из белков коронавируса (как правило, S-белок), против которого вырабатываются антитела и клеточный иммунитет. К российским векторным вакцинам относится «Спутник V» и «Спутник Лайт».
- Пептидные. В данном случае используются уже готовые очищенные белки коронавируса. Российская «ЭпиВакКорона» представляет собой химически синтезированные пептидные компоненты S-белка коронавируса.
- Цельновирионные. Вакцины с ослабленными или инактивированными (убитыми) вирусными частицами. К цельновирионным вакцинам относится «КовиВак».
Российские вакцины: что выбрать?
«В России в качестве первой вакцины стоит выбирать только «Спутник V». Это единственная вакцина с опубликованными данными и доказанной эффективностью и безопасностью. Эффективность «КовиВака» не ясна. Публикаций нет. По результатам групп добровольцев, антител вырабатывается крайне мало, а это показатель степени активации иммунитета. «ЭпиВакКорона» – неудачная вакцина. После нее не образуются нейтрализующие антитела. Статья об эффективности вакцины, которую опубликовал Роспотребнадзор после вакцинации своих сотрудников, показала, что люди тяжело болели, и чаще, чем в среднем за этот период по Москве. То есть защиты «ЭпиВакКорона» не давала».
Дуднакова Татьяна Валерьевна
эксперт
научный сотрудник Университета Эдинбурга, Великобритания
«Гам-КОВИД-Вак» («Спутник V»)
Тип вакцины: векторная
Дата регистрации в РФ: 11 августа 2020
Схема вакцинации: 2 дозы с интервалом 21 день
Эффективность: 91,6%
Стадия испытаний: 3 и 4 фазы (промежуточные результаты исследований ожидаются осенью 2021 года)
«Гам-КОВИД-Вак» («Спутник V») – комбинированная векторная вакцина, разработанная Национальным исследовательским центром эпидемиологии и микробиологии имени Н.Ф. Гамалеи. Из-за сложившейся экстраординарной ситуации вакцину пришлось зарегистрировать уже после II фазы испытаний, чего ранее не было¹.
Фазы исследований препаратов
Обычно на поиск вакцины к конкретному возбудителю (вирусу или бактерии) уходит от 5 до 15 лет и больше. Однако вакцины нового поколения возможно создать гораздо быстрее. Например, если ученые берут уже испробованную и изученную векторную основу для вакцины, как было у разработчиков «Спутника V». В этом случае на то чтобы встроить в нее ген одного из белков возбудителя инфекции, к которому потом и выработается иммунитет, требуется всего около двух недель. Наиболее долгосрочные клинические испытания, в которых в несколько этапов изучают иммуногенность, безопасность и эффективность вакцины.
На первой фазе исследований препарат вводят 10-30 добровольцам; на второй – 50-500; на третьей же фазе принимает участие более 1000 человек разного возраста.
На оценку эффективности и безопасности исследуемого препарата уходит от полугода до нескольких лет, поскольку надлежит выяснить как краткосрочные, так и долгосрочные эффекты вакцины. В частности, как долго она защищает человека от патогена, есть ли побочные эффекты.
Уже после регистрации и начала применения препарата наступает IV фаза исследований. Разработчик обязуется собирать новую информацию об эффектах препарата (например, редкие побочные явления) уже после выхода на рынок. Это касается не только вакцин, но и всех препаратов.
В качестве вектора для «Спутника V» используется аденовирус человека, в геном которого вставлен ген фрагмента S-белка коронавируса. Примечательно, что векторы первой и второй дозы «Спутник V» отличаются. Первый компонент изготовлен на основе аденовируса 26 серотипа, а второй – аденовируса 5 серотипа. Такой подход не случаен. Дело в том, что после прививки иммунитет вырабатывается как против коронавирусного S-белка, так и против белков оболочки аденовируса (вектора). Это значит, что повторное введение такого же вектора будет малоэффективно, поскольку иммунитет его быстро разрушит. Поэтому второй компонент «Спутника V» изготовлен на основе другого вектора.
В ноябре 2021 года был опубликован первый промежуточный анализ данных третьей фазы клинических испытаний в России. Заявленная эффективность препарата «Спутник V» составила 92%. Позже, в феврале 2021, в журнале The Lancet были опубликованы полные промежуточные результаты третьей фазы, согласно которым эффективность «Спутника V» составляет 91,6% после двукратного введения².
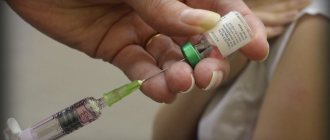
Вакцины «Гам-КОВИД-Вак» и «Спутник Лайт». Фотографии Максима Мишина с сайта мэра и правительства Москвы: https://www.mos.ru/mayor/media/photo/8049057/tiles/2/15/ и https://www.mos.ru/news/item/92820073/
«Спутник Лайт»
Тип вакцины: векторная
Дата регистрации в РФ: 6 мая 2021
Схема вакцинации: 1 доза
Эффективность: 79,4%
Стадия испытаний: 3 и 4 фазы (промежуточные результаты исследований ожидаются осенью 2021 года)
«Спутник Лайт» – это первый компонент вакцины «Спутник V». Эффективность препарата составляет 79,4% (после одной дозы). Это своего рода экспресс-прививка. Идея однокомпонентной вакцины заключается в том, чтобы охватить как можно больше населения, дав ему хоть какую-то защиту от ковида.
На практике же получилось так, что далеко не все в России желают прививаться. Нехватки вакцин в стране нет. Поэтому некоторые эксперты полагают, что «Спутник Лайт», возможно, пригодится для ревакцинации (третья доза вакцины для усиления иммунитета).
Преимущества и недостатки векторных вакцин
У векторных вакцин типа «Спутник V» и «Спутник Лайт» имеются свои сильные и слабые стороны. Теоретически они должны работать так же эффективно, как и живые вакцины (на основе ослабленных вирусов).
Проблема живых вакцин в том, что никто не знает, как вирус мутирует на этапе производства такого препарата. Всегда есть вероятность, что ослабленный вирус сможет вернуть себе былую силу, и тогда прививка превратится в настоящую инфекцию. С векторными вакцинами такой опасности нет, поскольку в качестве векторов используются безопасные для человека модифицированные вирусы, которые не мутируют.
Одним из предубеждений против векторных вакцин является якобы их малая изученность. Однако это не так. Аденовирусы стали изучать для применения в медицине уже более 50 лет назад. Первыми были живые вакцины от аденовирусных инфекций, варианты которых до сих пор используют в армии США. Но очень быстро стало ясно, что аденовирус, лишенный возможности репликации, является удобным вектором для доставки генетических конструкций в клетки. Поскольку аденовирусы не могут встраиваться в ДНК-клетки хозяина, использование их как векторов доставки безопасно и эффективно. Аденовирусы применяются также в онкотерапии.
Аденовирусы получили наибольшее распространение как основа для вакцин против коронавируса. Например, вакцина AZD1222 на основе аденовируса шимпанзе, разработанная учеными из Оксфорда, широко применяется сегодня в мире. Она чуть менее эффективна, чем российский «Спутник V».
Недостатком векторных вакцин является тот факт, что кроме ответа к спайк-белку вырабатывается иммунитет к белкам оболочки аденовируса. Иммунитет к аденовирусам нестойкий, но еще не ясно сколько раз можно повторять такую вакцинацию. Пока же по опыту Великобритании с вакциной AstraZeneca и опыту групп добровольцев «Спутника V» мы знаем, что ревакцинация аденовирусной прививкой эффективна, если произвести ее минимум через 3 месяца после вакцинации. Однако неизвестно, сколько раз ее можно повторить. В то же время очевидно, что прививки от ковида могут стать ежегодной обыденностью.
«КовиВак»
Тип вакцины: цельновирионная инактивированная
Дата регистрации в РФ: 19 февраля 2021
Схема вакцинации: 2 дозы с интервалом 2 недели
Эффективность: не установлено (еще на стадии исследования)
Стадия испытаний: 3 фаза (промежуточные результаты исследований ожидаются 30 декабря 2021 года)
Инактивированную вакцину против нового коронавируса создали в Федеральном научном центре исследований и разработки иммунобиологических препаратов им. М. П. Чумакова. К концу 2020 года удалось завершить все доклинические исследования (на культурах клеток и животных) и начать клиническую фазу испытаний.
Вирус для производства вакцины «КовиВак» был выделен у больного, который проходил лечение в ГКБ №40 (Коммунарка). Выделенный вирус затем культивировали (размножили) на клеточных культурах и убили химическим реагентом – бета-пропиолактоном.
Ежегодно планируется выпускать до 10 миллионов доз «КовиВака». При этом 3 фаза клинических исследований все еще продолжается. В ней принимает участие 3000 добровольцев. Завершить исследование планируют к концу 2021 года, после чего станет понятно, насколько эта вакцина эффективна и безопасна.
Преимущества и недостатки инактивированных вакцин
Преимущество инактивированных вакцин перед живыми заключается в отсутствии риска инфицирования. Убитые вирусы не могут мутировать, соответственно – в них нет потенциальной опасности.
- Преимущество по сравнению с векторными и мРНК-вакцинами в том, что пациенту вводится цельный вирус. Это приводит к формированию иммунитета против всех вирусных белков, а не только фрагмента S-белка. Ранее считалось, что S-белок консервативен и не будет меняться у мутировавших штаммов. Но на практике мы наблюдаем иное. Это приводит к снижению эффективности как векторных, так и мРНК-вакцин, нацеленных исключительно на S-белок.
- У инактивированных вакцин есть и недостатки. Они формируют неполноценный противовирусный иммунитет. Связано это с тем, что они не в состоянии проникнуть в клетку (а вирусы – это внутриклеточные паразиты), и не могут сформировать Т-клеточный иммунный ответ. Поэтому для усиления их эффективности применяются адъюванты. У вакцины «КовиВак» это гидроксид алюминия.
- Кроме того, при химической обработке часть белков теряет свою структуру, в том числе шиповидный белок, в результате чего теряется много эпитопов. В группах добровольцев было замечено, что после «КовиВак» вырабатывается значительно меньше антител к шиповидному белку, а именно к ним относятся нейтрализующие антитела, защищающие от инфекции. Теоретически у инактивированных вакцин повышен риск образования аутоиммунных реакций, но эти опасения с «КовиВаком» пока не оправдались. Серьезные недостатки цельновирионных вакцин – необходимость наращивать большие объемы опасного возбудителя и сложности масштабирования производства вакцины, когда для каждой партии необходимо подбирать условия химического воздействия индивидуально. Аналогичную вакцину, разрабатываемую в Шотландии, в результате решили не пускать в производство. Главным недостатком инактивированных вакцин против коронавируса (это мы можем наблюдать на примере китайских аналогов) является их более низкая эффективность по сравнению с векторными и РНК- вакцинами.
«ЭпиВакКорона»
Тип вакцины: пептидная
Дата регистрации в РФ: 6 мая 2021
Схема вакцинации: 2 дозы с интервалом 14-21 день
Эффективность: не установлена
Стадия испытаний: 3 фаза (оглашение результатов исследований планируется летом 2021 года)
«ЭпиВакКорона» – разработка Государственного научного центра вирусологии и биотехнологии «Вектор». Вакцина представляет собой суспензию, в составе которой три небольших белковых фрагмента (пептида) S-белка коронавируса.
«ЭпиВакКорону» стали применять до окончания второй фазы клинических испытаний3. Третья фаза началась в конце 2021 года и продолжается по сегодняшний день. Результаты исследований планируют огласить осенью 2021 года (сроки неоднократно переносились разработчиком).
Как и в случае с инактивированными вакцинами, в состав пептидных также входит адъювант (гидроксид алюминия) – вещество, усиливающее иммунный ответ.
Что касается эффективности «ЭпиВакКороны», то вопрос остается открытым. Промежуточные результаты второй фазы исследований были опубликованы в российском журнале «Инфекция и иммунитет», где было заявлено о 100% эффективности препарата. Однако у критиков большие сомнения на этот счет, поскольку импакт-фактор (показатель цитирований) этого журнала всего 0,68. Для сравнения, IF журнала The Lancet (в котором были опубликованы данные по «Спутнику V») – 60,4, что почти в 100 раз больше.
Преимущества и недостатки пептидных вакцин
Преимущество белковых вакцин в том, что их можно быстро протестировать. Они считаются более безопасными, по сравнению с остальными прививками.
Проблема белковых вакцин в сложности наработки пептидов. Кроме того, такие препараты не отличаются высокой эффективностью. Скорее всего, иммунитет от пептидных вакцин будет нестойким и пациенту потребуется ревакцинация.
Наша иммунная система и активные ингредиенты
Активный ингредиент в вакцине обычно производится из вирусного или бактериального патогена. Существует два различных подхода к этому, причем патоген либо жив, либо инактивирован. Вакцины, содержащие живые бактерии или вирусы, называются живыми аттенуированными вакцинами
. Патоген ослаблен, но еще способен вызвать сильный иммунный ответ.
Живые аттенуированные вакцины для всех не подходят. Если у человека ослаблен иммунитет, он может заболеть той болезнью, от которой его должна защищать вакцина.
В связи с этим чаще в вакцинах используют инактивированную версию активных ингредиентов, принимающих форму целых бактерий или вирусов, которые были убиты. Однако большинство вакцин на самом деле являются бесклеточными
, что означает, что они не содержат всего патогенного организма. Вместо этого они состоят из частей патогена, таких как белки или молекулы сахара. Наш организм распознает эти молекулы как чужеродные и вырабатывает иммунный ответ.
Примерами бесклеточных вакцин являются:
- анатоксиновые вакцины, содержащие инактивированные токсины из патогенных бактерий
- конъюгированные вакцины изготавливают из комбинации патоген-специфических молекул сахара и анатоксиновых белков, так как сами сахара не вызывают достаточно сильных иммунных реакций
- рекомбинантные вакцины, изготовленные с использованием бактерий или дрожжевых клеток, чтобы сделать много копий определенных молекул из патогена
Иностранные вакцины
Иностранные вакцины от коронавируса. Фото: marcbruxelle / Depositphotos
Самыми популярными иностранными вакцинами являются мРНК-препараты от Pfizer/BioNTech и Moderna, векторная вакцина от AstraZeneca, а также китайские цельновирионные препараты от Sinovac и Sinopharm.
Pfizer/BioNTech и Moderna – первые в мире мРНК-вакцины
Разработчики вакцин от Pfizer/BioNTech и Moderna решили пойти другим путем в решении проблем с коронавирусом. Принципиальное отличие мРНК-вакцин в том, что вирусные белки синтезируются в организме человека. Матричная РНК (мРНК) – это своего рода инструкция, прочитав которую клетка начинает производить закодированный белок4. В данном случае это фрагмент S-белка коронавируса.
Сегодня мРНК-вакцины против коронавируса применяются в США, Великобритании, Евросоюзе, Израиле, Украине и многих других странах. Предварительные результаты показывают хорошую защиту от госпитализаций и смертельных исходов. В частности, в США (где привито больше 55% населения) уже говорят об эпидемии не привитых. Подавляющее большинство пациентов, попадающих в госпитали с ковидом, это люди, не прошедшие вакцинацию.
Преимущества и недостатки мРНК-вакцин
Вакцины на основе матричной РНК отличаются высокой эффективностью, поскольку они проникают внутрь клетки. Имитация инфицирования вирусом приводит к формированию полноценного иммунитета. Для таких препаратов не нужны адъюванты. Кроме того, мРНК-вакцины можно быстро наработать. Если живые или инактивированные вакцины нужно выращивать на клеточных культурах, то мРНК-препараты «печатаются» на специальных синтезаторах. В экстренных условиях, когда за короткое время необходимо привить большое количество людей, это рациональный подход.
Недостаток мРНК-препаратов – в недостаточной изученности. Это новые вакцины, которые ранее никогда не применялись. Данных о долгосрочном влиянии таких прививок на здоровье человека пока нет.
Векторная вакцина от AstraZeneca
Это вакцина, изготовленная по такому же принципу, как и «Спутник V». В данном случае в качестве вектора используется модифицированный вирус шимпанзе5.
Эффективность векторной вакцины от AstraZeneca составляет 79% от симптоматической и 100% от тяжелой формы COVID-19. Это основная вакцина, которой прививаются страны ЕС. Весной 2021 года некоторые государства временно приостанавливали вакцинацию этим препаратом из-за данных о тромбозе и других тяжелых последствиях. Однако вскоре европейские регулирующие органы вновь разрешили вакцинацию.
Рисунок 1. Виды вакцин против COVID-19. Источники: Роспотребнадзор и ВОЗ (WHO): https://www.rospotrebnadzor.ru/about/info/news/news_details.php?ELEMENT_ID=15468, https://www.who.int/ru/news-room/feature-stories/detail/the-race-for-a-covid-19-vaccine-explained
Цельновирионные вакцины от Sinopharm и Sinovac
Крупными поставщиками вакцин от коронавируса стали китайские биофармацевтические компании Sinopharm и Sinovac. Они разработали цельновирионные противоковидные вакцины по типу «КовиВака».
Помимо Китая, эти вакцины активно применяются в Турции, Чили, Объединенных Арабских Эмиратах, Аргентине и других странах. Результаты третьей фазы исследований в разных странах колеблется от 50 до 84%6.При этом вакцины на 100% эффективны в предотвращении тяжелых форм и смерти.
Ошибся? Признай!
«Разработка вакцин – сложное дело. Неудачи – это нормально, главное, их признать. «ЭпиВакКорона» не работает, ее нельзя колоть, но она доступна для вакцинации. В мире было несколько нерабочих вакцин. Например, СаноФи института Пастера – белковая вакцина, в чем-то похожая на «ЭпиВакКорону». В ее составе – спайк-белок, экспрессированный в бакуловирусной системе. Немцы пытались сделать мРНК-вакцину, и это не получилось. В Шотландии разрабатывалась инактивированная цельновирионная вакцина, которую решили не вводить в оборот.
Инактивированные вакцины менее эффективны против ковида, чем ген-переносящие. Китайские цельновирионные инактивированные вакцины показали себя не очень хорошо, у них невысокая эффективность. Сейшелы и Чили, привившие население этими вакцинами, получили волну ковида с госпитализациями и смертями и были вынуждены срочно перепрививать население векторной вакциной AstraZeneca.
Векторные и мРНК-вакцины, используемые сегодня, высоко эффективны, они с большим отрывом оставили позади себя инактивированные варианты. По иммуногенности и эффективности вакцины идут так: Pfizer/BioNTech, Moderna, потом «Спутник V» и AstraZeneca».
Дуднакова Татьяна Валерьевна
эксперт
научный сотрудник Университета Эдинбурга, Великобритания
Быстро не значит плохо: почему вакцину от коронавируса разработали за короткие сроки?
Разработка и тестирование вакцины заняли около года. Это уникальный, но объяснимый, случай. Прежде всего, ускорило создание «Спутник V» то, что вакцина была сделана на основе аденовирусного вектора. Такая технология уже давно известна ученым, а сам центр им. Гамалеи имел опыт в выпуске подобных вакцин. Ранее была разработана вакцина от ближневосточного респираторного синдрома. Вирус, который его вызывает – MERS, также относится к группе коронавирусов.
Быстрое распространение и способность к мутации вируса требовали кардинальных решений. При этом безопасность и эффективность вакцины на первом месте. Именно поэтому первые фазы исследования были проведены с соблюдением всех международных правил: количество добровольцев на каждой фазе, критерии оценки их состояния здоровья после вакцинации. Только после того, как вакцина показала свою безопасность и способность защищать от коронавируса, было принято решение о массовой вакцинации.
Сравнение российских вакцин
Для удобства в таблице 1 приводим сравнительные характеристики российских вакцин против нового коронавируса.
Таблица 1. Сравнение российских вакцин против вируса SARS-CoV-2.
| Название | Состав препарата | Хранение | Иммуногенность | Эффективность | Побочные реакции | Способ и схема |
| «Спутник V» («Гам-КОВИД-Вак») | Рекомбинантные аденовирусы 26 и 5 серотипов с геном фрагмента S-белка коронавируса, соли для стабилизации препарата в растворе | При температуре не выше минус 18 ℃. Допускается хранение в жидком виде при температуре 2-8 ℃ | Клеточный и гуморальный иммунитет формируется на 42-й день после прививки. Согласно данным исследований, нейтрализующие антитела формируются у 98% людей | Общая эффективность – 91,6%. Для лиц старше 60-ти лет – 91,8% | Боль в месте инъекции. Симптомы, напоминающие грипп и простуду. Боли в мышцах и суставах, недомогание, головная боль | Инъекционная вакцина. 2 дозы с интервалом 21 день |
| «Спутник Лайт» | Рекомбинантный аденовирус 26 серотипа с геном фрагмента S-белка коронавируса, соли для стабилизации препарата в растворе | При температуре не выше минус 18 ℃. Допускается хранение в жидком виде при температуре 2-8 ℃ | Нейтрализующие антитела обнаруживаются у 96,9% людей на 28-й день после прививки | Заявленная эффективность – 79,4% после 1 дозы | Боль в месте инъекции. Симптомы, напоминающие грипп и простуду. Боли в мышцах и суставах, недомогание, головная боль | Инъекционная вакцина. Однократное введение |
| «КовиВак» | Антиген инактивированного коронавируса SARS-CoV-2, адъювант, соли для стабилизации препарата в растворе | При температуре 2-8 ℃. Замораживать вакцину нельзя | На стадии исследований | На стадии исследований | Инъекционная вакцина. 2 дозы с интервалом 14 дней | |
| «ЭпиВакКорона» | Химически синтезированные пептиды S-белка коронавируса, адъювант, соли для стабилизации препарата в растворе | При температуре 2-8 ℃. Замораживать вакцину нельзя | Предположительно, иммунитет формируется на 35-40-й день после полной вакцинации. Нейтрализующие антитела формируются у 82,1% людей | Не установлена. Теоретически может быть эффективна против разных штаммов, поскольку содержит консервативные пептиды S-белка коронавируса | Боль в месте инъекции. Кратковременное повышение температуры до 38-38,5 ℃ | Инъекционная вакцина. 2 дозы с интервалом 14-21 день |
Эффективность вакцин против новых штаммов коронавируса
Данные об эффективности существующих вакцин (российских и иностранных) противоречивы. Ведущие производители профилактических препаратов от COVID-19, такие как Pfizer, Moderna и AstraZeneca сообщают о сохранении высокой эффективности вакцин против штамма дельта. Речь идет о защите прививок от госпитализаций и смерти на уровне 90-96%. Согласно данным из Великобритании, против дельта-штамма эффективен и «Спутник V» (90% эффективности).
Что касается защиты от симптоматических форм ковида, то в Израиле эффективность препарата Pfizer/BioNTech составила 64%. Чуть позже Министерство здравоохранения Израиля заявило, что этот показатель снизился до 39%.
Учитывая вероятное снижение эффективности существующих препаратов против новых штаммов, производители задумываются о создании новых вакцин. Технологии останутся прежними (векторные, мРНК-вакцины), но прививки будут нацелены на другие компоненты вируса (которые не меняются при мутациях).
Как вакцина формирует приобретенный иммунитет?
При первом заражении инфекцией иммунной системе нужно некоторое время для выработки приобретенного иммунитета. Он работает эффективнее врожденного и может защищать нас на протяжении всей дальнейшей жизни, но формируется такой иммунитет не сразу.
Тот же принцип действует и при вакцинации. Упрощенно выработка приобретенного иммунитета происходит в четыре этапа:
- Индукция. Макрофаги атакуют чужеродные клетки и передают информацию об антигене лимфоцитам.
- Иммунорегуляторный этап. T- и B-лимфоциты нацеливаются на борьбу с инфекционным агентом.
- Эффекторная стадия. Происходит выработка специфических антител и Т-лимфоцитов против инфекции.
- Формирование иммунологической памяти, которая позволяет мгновенно отреагировать на вторжение возбудителя, против которого была сделана прививка.
На формирование защиты при этом уходит около месяца, поэтому прививку от гриппа или клещевого энцефалита делают заранее.
Противопоказания к вакцинации
Пользу и потенциальный риск вакцинации оценивает врач. Фото с сайта мэра и правительства Москвы https://www.mos.ru/mayor/themes/18299/6980050/
Перечень противопоказаний указан в инструкции конкретной вакцины. Внимательно прочитайте ее, а также проконсультируйтесь с врачом, прежде чем вакцинироваться. Рассмотрим основные противопоказания к существующим российским вакцинам.
Самые известные мифы о прививках
Вокруг безопасности вакцин всегда было много слухов, и некоторые из них породили очень живучие мифы, несмотря на то, что никаких доказательств их правдивости нет. Интересно, что мифы об опасности вакцин воспринимаются многими людьми серьезнее, чем реальная угроза, исходящая от инфекций. Мы уже забыли, чем страшны корь, коклюш и полиомиелит. Нам кажется, что эти болезни уже не вернутся, а потому мы начинаем бояться прививок сильнее, чем болезней.
Правда ли, что вакцины вызывают аутизм?
Это распространенный миф. В 1998 году в журнале Lancet была опубликована статья о связи между вакциной против кори, краснухи и паротита (свинки) и аутизмом. Позже приведенные в ней данные были признаны недостоверными: часть из них была фальсифицирована автором статьи Эндрю Уэйкфилдом. В 2010 году его лишили врачебной лицензии за нарушение профессиональной этики.
Правда ли, что с помощью вакцины можно чипировать человека?
Чипирование (введение электронного чипа) людей с помощью прививок технически невозможно. Часто в одном флаконе находится несколько доз препарата. Даже если в нем есть микрочипы, невозможно дозировать их, набирая раствор шприцем из флакона. Если в ампуле содержится одна доза вакцины, вводимый с препаратом чип должен иметь размеры меньше диаметра иглы для инъекций. Но в этом случае он может остаться на стенках флакона со следами жидкости, а значит, нет гарантии, что чипирование произойдет. Производство вакцин выполняется под очень строгим контролем, и попадание любых посторонних компонентов в препарат исключено.
«Спутник V» и «Спутник Лайт»
Абсолютные противопоказания
Препараты «Спутник V» и «Спутник Лайт» противопоказаны в следующих случаях:
- повышенная чувствительность к какому-либо компоненту препарата (или аналогичных препаратов, содержащих те же компоненты);
- тяжелая аллергия в анамнезе;
- инфекционные и неинфекционные заболевания на стадии обострения (прививаться можно спустя 2-4 недели после выздоровления или наступления ремиссии);
- беременность и грудное вскармливание (вопрос на стадии обсуждения);
- возраст до 18 лет (проходят клинические исследования для подростков).
Если тяжелые неблагоприятные симптомы (например, сильная аллергическая реакция) возникли после первой дозы препарата, то вторая доза противопоказана. В некоторых случаях врач рассматривает вопрос о повторной вакцинации другим препаратом («КовиВак» или «ЭпиВакКорона»), но не ранее, чем через 3 месяца после введения первой дозы «Спутника».
Прививать с осторожностью
При некоторых хронических заболеваниях «Спутник V» и «Спутник Лайт» применяют только после консультации врача, который внимательно изучает историю болезни пациента. К таким заболеваниям относятся:
- хронические болезни печени и почек;
- болезни эндокринной системы (сахарный диабет, тяжелые нарушения щитовидной железы);
- тяжелые патологии органов кроветворения;
- эпилепсия;
- острое нарушение мозгового кровообращения;
- воспалительные заболевания сердца (миокардит, эндокардит и перикардит);
- злокачественные опухоли;
- аутоиммунные заболевания.
В таких случаях задача врача – оценить пользу и потенциальный риск вакцинации.
«КовиВак»
Абсолютные противопоказания
Цельновирионную вакцину «КовиВак» нельзя вводить при следующих обстоятельствах:
- если раньше была тяжелая реакция на любую из вакцин (например, температура до 40 ℃, отечность, тяжелая аллергическая реакция, судороги);
- при наличии в анамнезе тяжелых аллергических реакций (анафилактический шок, отек Квинке, экзема);
- беременность и кормление грудью;
- возраст до 18 лет.
Прививать с осторожностью
«КовиВак» нельзя использовать при некоторых острых и хронических заболеваниях на стадии обострения. К таковым относятся:
- острые инфекции;
- хронические инфекции на стадии обострения;
- хронические патологии внутренних органов (печени, почек, сердца, легких, органов ЖКТ);
- иммунные нарушения.
«КовиВак» и иммунодефицит
Пациентам с иммунодефицитными состояниями «КовиВак» НЕ противопоказан. Однако у людей, принимающих иммунодепрессанты (препараты, подавляющие иммунитет), эффективность прививки может снизиться. Если это возможно, то такие препараты желательно отменить в течение месяца до и после прививки. Решение о такой коррекции в лечении принимает только лечащий врач.
«ЭпиВакКорона»
Абсолютные противопоказания
Пептидную вакцину «ЭпиВакКорона» нельзя применять в следующих случаях:
- повышенная чувствительность к компонентам препарата;
- тяжелые аллергические заболевания;
- острые и хронические (в стадии обострения) патологии;
- первичный иммунодефицит (наследственное заболевание, приводящее к нарушению работы иммунной системы);
- злокачественные опухоли;
- болезни крови;
- возраст до 18 лет.
Прививать с осторожностью
При некоторых заболевания и состояниях вакцинировать пациента можно только после консультации врача. К таким болезням относятся:
- болезни печени и почек;
- эндокринные заболевания;
- тяжелые патологии центральной нервной системы (эпилепсия, инсульт и другие);
- болезни сердца и сосудов;
- вторичные иммунодефициты (приобретенные при жизни);
- аутоиммунные заболевания;
- легкие или средние аллергические реакции.
Разработка вакцины от коронавируса. Фото: Минобороны России / YouTube:
В чем важность вакцинации для взрослых и детей
Механизм активной иммунизации предназначен для предупреждения массового распространения вирусных инфекций – кори, краснухи, гепатита, паротита, а также бактериальных – коклюша, дифтерии, столбняка и многих других.
Прививки необходимы для:
- профилактики инфицирования, снижения риска заболеть болезнями, опасными для жизни;
- защиты от смертельных неизлечимых заболеваний, например, бешенства, вируса папилломы человека;
- предупреждения серьезных осложнений, так как после прививки небольшой риск заболеть сохраняется, но болезнь будет протекать легче, а вероятность смерти уменьшается в несколько раз;
- создания иммунитета у большей части населения (не менее 2/3 от численности). Когда коллективный иммунитет сформирован, останавливается распространение инфекции, а новые случаи заражения не появляются.
Прививаться от некоторых инфекций необходимо не только в детском возрасте, но и во взрослом, так как со временем иммунитет ослабевает и нуждается в дополнительном стимулировании. Ревакцинация взрослого населения важна, потому что детские инфекции переносятся им гораздо тяжелее и чаще вызывают осложнения.
Прививки взрослым обязательны при перемещении по регионам и при путешествиях в страны с неблагоприятной эпидемиологической обстановкой.
Лицам с хроническими болезнями вакцинация показана для предупреждения осложнений.
Детям прививки необходимы с целью профилактики тяжелых инфекционных заболеваний, сложно поддающихся лечению и вызывающих опасные для жизни осложнения.
Побочные эффекты
Легкие и умеренные побочные эффекты от вакцин считаются вариантом нормы. Вы не должны беспокоиться, если после прививки повысилась температура, появились симптомы простуды или гриппа. В течение нескольких дней такие реакции исчезают самостоятельно.
К самым частым побочным эффектам после вакцинации против нового коронавируса относятся:
- боль в месте инъекции (может болеть все плечо);
- повышение температуры тела;
- гриппоподобные симптомы;
- головная боль;
- боль в мышцах и суставах;
- диарея (понос).
По всем правилам вакцинации после прививки пациент должен оставаться в медицинском учреждении еще 20-30 минут. Это нужно для того чтобы оказать пациенту помощь, если вдруг разовьется аллергическая реакция.
В США, Великобритании и некоторых других странах ведется открытый реестр побочных эффектов от вакцинации. Среди очень редких, но тяжелых последствий отмечают миокардиты (воспаление сердца) и тромбозы (закупорка сосудов тромбами). От российских вакцин подобных эффектов не зарегистрировано. Здесь нужно учесть тот факт, что Россия не ведет открытый реестр побочных эффектов.
Что касается долгосрочных побочных эффектов ковид-вакцин, то информация собирается в режиме реального времени. Спустя почти год после начала масштабных клинических исследований, долгосрочных побочных эффектов пока не установлено.
Вакцина и прививка — одно и то же?
Прививка по своему определению — это процесс введения вакцины, этот термин произошел от глагола “прививать” и является синонимом вакцинации. Прививки делают по определенному графику, их отмечают в медицинской карте или прививочном сертификате. Соблюдать график прививок следует всем, особенно это касается людей, которые живут в тесных коллективах. В детских садах, школе или армии условия прекрасно подходят для распространения многих серьезных инфекций, передающихся воздушно-капельным путем или через еду и посуду.
Важно! При прививке от одной и той же болезни могут использоваться разные вакцины, например, детские препараты не всегда подходят для взрослых. Часто одна вакцина защищает сразу от нескольких заболеваний (как вакцина АКДС против коклюша, дифтерии и столбняка). Это помогает сократить количество инъекций и походов к врачу.
Источники
- Минздрав России зарегистрировал первую в мире вакцину от COVID-19. Министерство здравоохранения Российской Федерации (11.08.2020). Дата обращения: 11 августа 2021. Архивировано 12 августа 2021 года.
- Logunov D. Y. et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia (англ.) // The Lancet. — 2021. — 2 February. — ISSN 0140-6736. — doi:10.1016/S0140-6736(21)00234-8
- Регистрационное удостоверение и Инструкция по медицинскому применению лекарственного препарата «ЭпиВакКорона вакцина на основе пептидных антигенов для профилактики COVID-19» от 13.10.2020 г. + Изменение № 1 от 13.01.2021 г. + Изменение № 2 от 10.02.2021 г. + Изменение № 3 от 03.03.2021 г. // Электронные образы документов на сайте «Государственный реестр лекарственных средств».
- Clinical trial number NCT04368728 for «NCT04368728: Study to Describe the Safety, Tolerability, Immunogenicity, and Efficacy of RNA Vaccine Candidates Against COVID-19 in Healthy Individuals» at ClinicalTrials.gov
- University of Oxford. A Phase 2/3 Study to Determine the Efficacy, Safety and Immunogenicity of the Candidate Coronavirus Disease (COVID-19) Vaccine ChAdOx1 nCoV-19. — clinicaltrials.gov, 2020-12-08. — № NCT04400838.
- Tanriover MD, Doğanay HL, Akova M, Güner HR, Azap A, Akhan S, Köse Ş, Erdinç FŞ, Akalın EH, Tabak ÖF, Pullukçu H, Batum Ö, Şimşek Yavuz S, Turhan Ö, Yıldırmak MT, Köksal İ, Taşova Y, Korten V, Yılmaz G, Çelen MK, Altın S, Çelik İ, Bayındır Y, Karaoğlan İ, Yılmaz A, Özkul A, Gür H, Unal S; CoronaVac Study Group. Efficacy and safety of an inactivated whole-virion SARS-CoV-2 vaccine (CoronaVac): interim results of a double-blind, randomised, placebo-controlled, phase 3 trial in Turkey. Lancet. 2021 Jul 17;398(10296):213-222. doi: 10.1016/S0140-6736(21)01429-X. Epub 2021 Jul 8. PMID: 34246358; PMCID: PMC8266301.
Элементы конструктора
Рисунок 3. Конструкция ДНК-вакцины на основе вектора pVAX1 с химерным геном (Rat cDNA, Human cDNA). Pcmv — цитомегаловирусный промотор; MCS — сайт для множественного клонирования генов; BGH pA — терминатор с сигналом полиаденилирования гена гормона роста быка; Kanamycin — ген устойчивости к канамицину; pUC ori — участок начала репликации плазмид группы pUC; HindIII, BstEII, XbaI — сайты рестрикции. Рисунок из [5].
Чтобы пригодиться для создания ДНК-вакцин, каждый уважающий себя вектор должен содержать необходимые конструкционные элементы (рис. 3).
- Структуры, обеспечивающие репликацию плазмиды (используются ori pUC19, pMB1), и сайты рестрикции.
- Селективные маркеры: гены устойчивости к антибиотикам (но не к пенициллину и другим β-лактамным антибиотикам) [5].
- СpG-мотивы бактерий, которые из-за отсутствия метилирования способны усиливать иммунную реакцию. Данный принцип лежит в основе разработки универсальной вакцины и подразумевает использование не генов, кодирующих белки-антигены микробов, а бактериальных последовательностей CG в качестве активного компонента вакцины [7].
- Последовательность Козак — консенсусная последовательность, окружающая старт-кодон (GCC(A/G)CCAUGG), которая играет важную роль в инициации трансляции у эукариот.
- Промотор для экспрессии целевого гена в клетках эукариот. Наиболее часто используют промоторы вируса SV40, цитомегаловируса (часто вместе с интроном А), промотор бета-актина, промоторы, специфичные для определенных видов ткани (например, промотор гена десмина для экспрессии в миоцитах, промотор гена гидроксилазы витамина D3 — в кератиноцитах, альбуминовый — в гепатоцитах). Применение промотора и системы синтеза бактериофага Т7 позволяет осуществлять экспрессию целевого гена без участия транскрипционной системы клеток макроорганизма и, соответственно, без перемещения вектора в ядро [8].
- Целевой ген, кодирующий белок патогена. Он также может содержать дополнительные нуклеотидные последовательности, кодирующие лиганды для рецепторов антигенпредставляющих клеток. Такими последовательностями могут выступать гены маркерного белка CD40, внеклеточного домена Fms-подобной тирозинкиназы-3 или антигена-4 Т-киллеров. Облегчение деградации антигена в протеасоме или лизосоме также будет стимулировать иммунную реакцию. Поэтому для усиления протеолитического расщепления антигена в его последовательность встраивают сигнал убиквитинирования [9, 10].
- После целевого гена следуют сигналы полиаденилирования, например, вируса SV40, гена β-глобина кролика или гормона роста быка.
- Замыкают эту цепочку стоп-кодоны, причем часто используются двойные или тройные терминирующие последовательности (TAGTGATGA).