Чем на самом деле является вакцина от коронавируса? Испытания, скрытые компоненты и правда о сроках разработки «Спутник V»
5 февраля 2021г.
Технология, которая легла в основу разработки вакцины «Спутник V» давно известна науке. Принцип ее действия прост: аденовирус, лишенный возможности размножаться, играет роль доставщика кусочка гена SARS-CoV-2. Впервые аденовирусный вектор использовался 40 лет назад в создании вакцины против лихорадки Эболы.
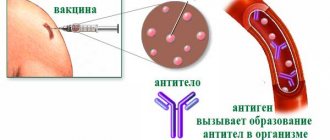
Институт им. Гамалеи, где и был синтезирован «Спутник V», создавал вакцины на основе аденовируса с 2015 г., поэтому ученым в относительно небольшие сроки удалось создать вакцину от коронавируса. Она защищает организм от заражения следующим образом: в аденовирусный вектор (вирус), который искусственно лишили возможности размножаться, вшили ген, кодирующий S-белок шипа коронавируса. Вектор доставляет кусочек РНК-вируса в клетку, а та, в свою очередь, реагирует на это так же, как реагировала бы на вторжение SARS-CoV-2. Начинают вырабатываться специфические антитела, которые и создают иммунитет против коронавируса.
Что входит в состав вакцины от коронавируса и содержатся ли в ней опасные «ингредиенты»?
Аденовирусный вектор – основное действующее вещество вакцины. Это главное составляющее, но, для работы прививки необходимы и другие компоненты. Они помогают сохранить эффект действующего вещества и облегчают его проникновение в клетки человека.
Помимо самого аденовирусного вектора в состав «Спутник V» входят:
- Трис – соединение, которое поддерживает необходимую для действия вакцины кислотность (pH).
- Натрия хлорид (или физиологический раствор) – им разбавляется лекарственное вещество, для увеличения его доступности для клеток.
- Магния хлорида гексагидрат – вводится в состав вакцины для восстановления и поддержания количества воды во внеклеточном и внутриклеточном пространстве. Это необходимо, чтобы предотвратить обезвоживание клеток.
- ЭДТА (Этилендиаминтетрауксусная кислота) – используется для сохранения генетического кусочка SARS-CoV-2, вшитого в аденовирусный вектор, так как РНК нестабильна вне вируса.
- Полисорбат – связывает компоненты вакцины.
- Сахароза, этанол и вода – для стерильности вакцины и лучшего ее «усвоения» клетками
Каждый «ингредиент» прививки от коронавируса абсолютно безвреден. Для того чтобы проверить, формируют ли в связке все эти компоненты устойчивый иммунитет к коронавирусу, проводятся испытания.
Какие испытания прошла вакцина от коронавируса?
Сразу после синтеза нового препарата, ученые провели доклиническое тестирование на хомячках и приматах. Проверяли токсичность, безопасность и эффективность новой вакцины. Никаких осложнений, побочных реакций у животных не возникло, поэтому ученые приступили к клиническим испытаниям на людях.
Первая фаза испытаний обычно проводится на небольшой группе здоровых добровольцев. Для тестирования российской вакцины «Спутник V» было привлечено 76 военных возрастом от 18 до 60 лет. Фаза была разделена на два этапа.
Первый этап длился 28 дней. Девятнадцати добровольцам поставили первую часть вакцины, основанной на ослабленном аденовирусе 26 типа, другим девятнадцати – вторую, с аденовирусом 5 типа. Так была проверена безопасность обоих компонентов вакцины. Результатом этапа стала хорошая переносимость препарата всеми добровольцами. Побочные эффекты были легкими или умеренными:
- боль в месте инъекции (58%);
- повышение температуры (50%);
- головная боль (42%);
- слабость (28)%;
- боль в мышцах и суставах (24%);
Опасных для жизни побочных эффектов обнаружено не было.
Во время второго этапа исследовался уже формирующийся после вакцинации иммунитет. Все добровольцы получили обе части вакцины с разницей в 21 день между ними. На 28 день после введения второй дозы, с помощью высокоточных тестов, у 100% добровольцев были обнаружены антитела к SARS-CoV-2. Более того, было доказано формирование другого – клеточного иммунитета. Обычно он сохраняется в «памяти» организма несколько лет.
Спустя три месяца после старта третьей фазы клинических испытаний в декабре 2021 г. российский Минздрав принял решение совместить последний этап исследований с массовой вакцинацией населения прививкой «Спутник V». Решение приняли оперативно, основываясь на предварительных результатах, опубликованных разработчиками вакцины в ноябре 2021 г.
В основе проведенных расчетов лежат случаи заболевания COVID-19 среди уже привитых добровольцев. Из общего числа участников испытаний, получивших обе положенные инъекции вакцины или плацебо (18 794), к концу третьей недели после второго укола вирус был диагностирован у 39 человек.
31 случай заражения был выявлен у тех, кто получил плацебо. В группе волонтеров, привитых настоящей вакциной, COVID-19 был диагностирован у восьмерых (группа получивших вакцину – в три раза больше группы плацебо). Сопоставление результатов по двум группам дает результат эффективности вакцины в 95%.
«Набранная группа участников исследований позволяет в полной мере исследовать профиль безопасности и профилактической эффективности вакцины на длительном промежутке времени», – пояснили в Минздраве.
Несмотря на то, что прививка «Спутник V» стала доступна всем желающим (за исключением группы с противопоказаниями), ученые продолжили наблюдение за добровольцами, принявшими участие в третьей фазе клинических испытаний. Второго февраля 2021г. разработчики вакцины представили результаты исследования в авторитетном медицинском издании The Lancet.
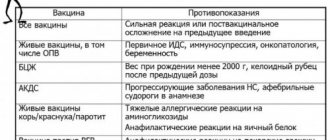
Противопоказания
Только врач может решить, подходит ли «Полимилекс» для вакцинации
«Полимилекс» противопоказан при наличии в анамнезе аллергической реакции на любой компонент вакцины.
Проведение вакцинации «Полимилекс» противопоказано в следующих случаях:
- Тяжелая реакция на предшествующее введение вакцины.
- Известная гиперчувствительность к одному или нескольким компонентам вакцины.
- Заболевание, сопровождающееся лихорадкой, острое инфекционное или хроническое заболевание в стадии обострения. Вакцинацию проводят через 2-4 недели после выздоровления или в период реконвалесценции или ремиссии. При нетяжелых ОРВИ, острых кишечных заболеваниях и др. прививки проводят сразу после нормализации температуры.
- Сильная реакция (температура выше 40 °С, отек и гиперемия в месте введения свыше 8 см в диаметре) или осложнение на предыдущее введение препарата.
Результаты последней третьей фазы клинических испытаний вакцины «Спутник V»
Третья фаза испытаний вакцины «Спутник V» длилась с 7 сентября по 24 ноября. В ней приняли участие 21 977 человек, из них 16 427 были привиты, а 5435 – получили плацебо (раствором, в который входят все ингредиенты «Спутник V», кроме самого аденовирусного вектора).
Согласно выводам ученых специфические антитела против коронавируса вырабатывались через 42 дня после первой прививки или через 21 день после второй у 95,8% добровольцев. Более того, в день первой инъекции и через 28 дней после второй у добровольцев уже определялся клеточный иммунитет.
Что касается побочных эффектов, они проявились у 7966 привитых, при этом у 94% из них были легкими и включали повышение температуры, неприятные ощущения в месте инъекции, головную боль и слабость. Лишь 0,3% привитых имели серьезные побочные эффекты, однако, независимая комиссия не доказала связи между ними и вакцинацией.
Эффективность вакцины при таких показателях составляет 91.6%.
«Спутник V» также исследовали на добровольцах старше 60 лет – всего 2144 человека. Эффективность вакцины в этой группе практически не отличается от общей и составляет 91.8%.
Таким образом, вакцина показала свою эффективность и безопасность как у людей от 18 до 60 лет, так и у пожилых добровольцев. При этом серьезных побочных эффектов, связанных с вакциной, обнаружено не было.
Биологические и иммунобиологические свойства Вакцина создает длительный иммунитет к вирусу полиомиелита типов 1, 2, 3 у большинства привитых (90-95%).
Назначение Активная профилактика полиомиелита. Плановым прививкам подлежат дети в возрасте от 3 месяцев до 14 лет.
Способ примененияВакцина предназначена для перорального применения. Ни при каких обстоятельствах данная вакцина не должна вводиться парентерально.
Прививки оральной полиомиелитной вакциной проводят 6 раз, в возрасте, установленном календарем профилактических прививок Возраст: 3 месяца 4,5 месяца 6 месяцев 18 месяцев 20 месяцев 14лет
Три первые прививки составляют курс вакцинации. Удлинение интервалов между прививками допускается в исключительных случаях, при наличии медицинских противопоказаний, укорочение интервалов между первыми тремя прививками не допускается. Допускается сокращение интервала между третьей и четвертой прививками до 3 месяцев, в том случае, если интервалы между первыми тремя прививками были значительно удлинены. Дети, прибывшие на данную территорию без документа о проведенных прививках, подлежат трехкратной иммунизации. Последующие вакцинации этих детей проводят в соответствии с возрастом.
Прививки по эпидпоказаниям проводят при возникновении заболеваний полиомиелитом в детском учреждении, населенном пункте. Контингент лиц, подлежащих иммунизации по эпидпоказаниям, и кратность прививок устанавливаются в каждом конкретном случае с учетом особенностей эпидемического процесса полиомиелита. В последующем очередные плановые прививки против полиомиелита проводят в установленные сроки.
Прививки против полиомиелита разрешается проводить в один день с вакцинацией АКДС-вакциной (АДС- или АДС-М анатоксином), допускается одновременное введение полиомиелитной вакцины с другими препаратами календаря прививок.
Вакцину применяют по 4 или 2 капли на прием в соответствии с расфасовкой препарата. Прививочную дозу вакцины закапывают в рот прилагаемой к флакону капельницей или пипеткой за 1 час до еды. Запивать вакцину водой или какой-либо другой жидкостью, а также есть или пить в течение часа после прививки не разрешается.
Неиспользованная вакцина из вскрытого флакона может храниться не более 2-х суток при температуре (6±2)°С во флаконе, плотно закрытом капельницей или резиновой пробкой. Разрешается при необходимости вакцину набирать стерильным шприцом через резиновую пробку при соблюдении правил асептики. В этом случае вакцина, оставшаяся во флаконе, может использоваться до конца срока годности.
Реакция на введение вакцины Реакция на введение вакцины практически отсутствует. У отдельных привитых, предрасположенных к аллергическим реакциям, чрезвычайно редко могут наблюдаться аллергические осложнения в виде сыпи типа крапивницы или отека Квинке. Крайнюю редкость как у привитых, так и у лиц, контактных с привитыми, представляют вакциноассоциированные заболевания, которые наблюдаются не чаще, чем 1 случай на 3 миллиона привитых детей. Они всегда требуют дифференциального диагноза с полиомиелитоподобными заболеваниями. Для ограничения циркуляции вакцинного вируса среди лиц, окружающих привитого ребенка, следует разъяснять родителям необходимость соблюдения правил личной гигиены ребенка после прививки (отдельная кровать, горшок, отдельные от других детей постельное белье, одежда и т.д).
Противопоказания Живая полиомиелитная вакцина является безопасным и ареактогенным препаратом. Противопоказаниями являются:
- Неврологические расстройства, сопровождавшие предыдущую вакцинацию полиомиелитной вакциной;
- Иммунодефицитное состояние (первичное), злокачественные новообразования, иммуносупрессия (прививки проводят не ранее, чем через 6 месяцев после окончания курса терапии);
- Плановая вакцинация откладывается до окончания острых проявлений заболевания и обострения хронических заболеваний. При нетяжелых ОРВИ, острых кишечных заболеваниях и др., прививки проводятся сразу же после нормализации температуры.
Условия хранения Хранитть в замороженном виде при температуре минус (20±1)°С в специальных низкотемпературных холодильниках или в жидком виде при (6±2)°С. Допустимо размораживание и повторное замораживание вакцины, но не более чем трехкратное на протяжении всего срока хранения. Срок годности При минус 20°С – два года, при темп. (6±2)°С- 6 месяцев.
Быстро не значит плохо: почему вакцину от коронавируса разработали за короткие сроки?
Разработка и тестирование вакцины заняли около года. Это уникальный, но объяснимый, случай. Прежде всего, ускорило создание «Спутник V» то, что вакцина была сделана на основе аденовирусного вектора. Такая технология уже давно известна ученым, а сам центр им. Гамалеи имел опыт в выпуске подобных вакцин. Ранее была разработана вакцина от ближневосточного респираторного синдрома. Вирус, который его вызывает – MERS, также относится к группе коронавирусов.
Быстрое распространение и способность к мутации вируса требовали кардинальных решений. При этом безопасность и эффективность вакцины на первом месте. Именно поэтому первые фазы исследования были проведены с соблюдением всех международных правил: количество добровольцев на каждой фазе, критерии оценки их состояния здоровья после вакцинации. Только после того, как вакцина показала свою безопасность и способность защищать от коронавируса, было принято решение о массовой вакцинации.